 Al momento de dar de alta a la orgullosa mamá con su recién nacido:
Al momento de dar de alta a la orgullosa mamá con su recién nacido:
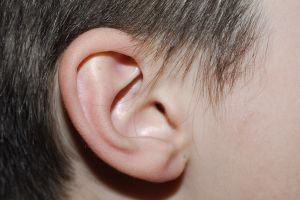
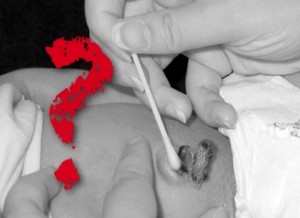
Mamá: «¿Cómo le limpio el ombligo?»
Pediatra: «Puedes hacerlo con un aplicador limpio de algodón y dejar que seque. Puedes usar agua y jabón»
Mamá: «¿y le pongo alcohol?»
Pediatra: «no es necesario»
Mamá intrigada: «¿en verdad?, ¿ni mertiolate ni nada?»
Pediatra: «de verdad, no es necesario. Sólo mantenlo limpio y seco»
¡Blasfemia! Imagínenlo. Años y años recomendando que se le ponga alcohol o algún antiséptico al muñón umbilical y salen con esto. De ser así, el doctor tendrá que pasar un bueeen rato explicando que realmente no es necesario.
Recuerdo cuando me topé con este artículo del American Family Physician hace unos 3 años. El artículo se acompaña de su panfleto informativo para el paciente. Su recomendación al familiar dice así: «No ponga alcohol en el cordón de su bebé. El cordón se secará y se caerá por sí solo dentro de las próximas 2 semanas».
La guía clínica de NICE dice así:»Debe recomendarse a los padres mantener el cordón limpio y seco, y que no se usen antisépticos de rutina».
Inclusive el texto para pacientes de eMedicine menciona que probablemente el pediatra recomendará que se limpie con alcohol el área unas 2-3 veces al día, pero que «algunas investigaciones» sugieren que el cordón se desprenderá más rápido si se deja en paz.
Finalmente tenemos una revisión Cochrane. Los autores incluyen 21 estudios, con un total de 8959 niños, la mayoría hechos en países desarrollados. Los resultados sugieren que da igual si se les pone antisépticos/antibióticos, si sólo se les limpia y seca, o si se les pone un placebo. ¿Sería igual en los países subdesarrollados? No sabemos, pero se me antoja pensar que sí.
Cuando tenemos frente a nosotros situaciones tan comunes como el cuidado del cordón umbilical del recién nacido, es difícil detenernos por un segundo y pensar ¿estará bien lo que siempre he recomendado? Si lo hacemos, y buscamos la evidencia, nos sorprenderemos de lo cambiante que es la medicina y tomaremos mejores decisiones para nuestros pacientes.
Giordano Pérez Gaxiola
Departamento de Medicina Basada en la Evidencia
Hospital Pediátrico de Sinaloa
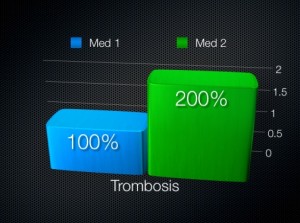
 Si un niño tiene reflujo vesicoureteral, está en mayor riesgo de infecciones de vías urinarias (IVU). Entonces, si le damos profilaxis con antibióticos debe disminuir el riesgo. ¿Cierto?
Si un niño tiene reflujo vesicoureteral, está en mayor riesgo de infecciones de vías urinarias (IVU). Entonces, si le damos profilaxis con antibióticos debe disminuir el riesgo. ¿Cierto? Los últimos dos números de la revista
Los últimos dos números de la revista